Aprox. 2000 a.C. - Los chinos usan
microscopios de agua hechos de una lente y
un tubo lleno de agua para visualizar lo
invisible. [1]
Aprox. 612 a.C. - Los asirios fabricaron las
lentes que sobreviven más antiguas del
mundo. [2]
1267 - Roger Bacon explica los principios de
la lente y propone la idea de telescopio y
microscopio. [3]
1590 - Los montadores de espectáculos
neerlandeses Hans Jansen y su hijo Zacharias
Jansen son reinvindicados por haber inventado
un microscopio compuesto por escritores
posteriores ( Pierre Borel 1620-1671 o 1628–
1689 y Willem Boreel 1591–1668)
1609 - Galileo Galilei desarrolla un
occhiolino (telescopio casero de 8 aumentos)
sentando las bases para el desarrolllo
posterior del [[microscopio compuesto].
1619 - Cornelius Drebbel (1572–1633)
presenta en Londres un microscopio
compuesto con dos lentes convexas.
1625 - Giovanni Faber de Bamberg
(1574-1629) de los Linceanos acuña la
palabra microscopio por analogía con
telescopio .
1665 - Robert Hooke publica Micrographia ,
una colección de micrografías biológicas y
acuña la palabra célula ( cell ) para las
estructuras que descubre en una corteza de
corcho .
1674 - Anton van Leeuwenhoek mejora un
microscopio e inventa el microscopio simple
para ver especímenes biológicos.
1863 - Henry Clifton Sorby desarrolla un
microscopio metalúrgico para observar la
estructura de meteoritos.
década de 1860 - Ernst Abbe descubre la
relación de senos de Abbe , un gran avance en
el diseño del microscopio, que hasta entonces
se basaba en gran medida en el ensayo y
error. La compañía de Carl Zeiss explotó este
descubrimiento y se convirtió en el fabricante
de microscopios dominante de su época.
1931 - Ernst Ruska comienza a construir el
primer microscopio electrónico . Se trata de un
microscopio electrónico de transmisión (en
inglés : Transmission electron microscope,
TEM)
1936 - Erwin Wilhelm Müller inventa el
microscopio de efecto de campo .
1938 - James Hillier construye otro TEM
1951 - Erwin Wilhelm Müller inventa el
microscopio de iones en campo y es el
primero en ver átomos.
1953 - Frits Zernike , profesor de física
teórica , recibe el Premio Nobel de Física por
su invención del microscopio de contraste de
fases .
1955 - George Nomarski , profesor de
microscopía , publicó las bases teóricas de
microscopía de contraste interferencial
diferencial. [4]
1965 - Manfred von Ardenne desarrolla el
primer microscopio electrónico de barrido .
1967 - Erwin Wilhelm Müller añade tiempo
de vuelo de espectroscopía al microscopio de
iones en campo , haciendo que la primera
sonda atómica y permitiendo la identificación
química de cada átomo individual.
1981 - Gerd Binnig y Heinrich Rohrer
desarrollan el microscopio de efecto túnel
( Scanning Tunneling Microscope , STM).
1986 - Gerd Binnig , Quate y Gerber
desarrollan el microscopio de fuerza atómica
( Atomic Force Microscope, AFM)
1988 - Alfred Cerezo , Terence Godfrey y
George D. W. Smith aplicó un detector sensible
a la posición a la sonda atómica, por lo que es
capaz de resolver átomos en 3 dimensiones.
1988 - Kingo Itaya inventa el microscopio
electroquímico de efecto túnel ( Electrochemical
scanning tunneling microscope )
1991 - Inventado el microscopio de fuerza
sonda Kelvin ( Kelvin probe force microscope ).
martes, 4 de noviembre de 2014
Historia del microscopio
Cromatogrfia
La cromatografía es un método físico de
separación para la caracterización de mezclas
complejas, la cual tiene aplicación en todas
las ramas de la ciencia. Es un conjunto de
técnicas basadas en el principio de retención
selectiva, cuyo objetivo es separar los distintos
componentes de una mezcla, permitiendo
identificar y determinar las cantidades de
dichos componentes. Diferencias sutiles en el
coeficiente de partición de los compuestos da
como resultado una retención diferencial sobre
la fase estacionaria y por tanto una
separación efectiva en función de los tiempos
de retención de cada componente de la
mezcla.
La cromatografía puede cumplir dos funciones
básicas que no se excluyen mutuamente:
Separar los componentes de la mezcla, para
obtenerlos más puros y que puedan ser usados
posteriormente (etapa final de muchas
síntesis).
Medir la proporción de los componentes de
la mezcla (finalidad analítica). En este caso,
las cantidades de material empleadas son
pequeñas.
Primeros auxilios
Secuencia de atención
Por ejemplo, al encontrar a una persona
inconsciente y con sospecha de haber recibido
una descarga eléctrica o electrocutación. La
persona que va a atender debe estar segura
que no será otra víctima. Si es seguro,
brindará la atención. De otro modo, debe
llamar al personal especializado en ayuda, sin
exponerse ella misma.
1. Evaluación inicial del paciente.
2. Valoración de la consciencia:
Se preguntará a la víctima cómo está, como se
encuentra. Si contesta, es símbolo inequívoco
de que respira y tiene pulso. En caso que no
conteste, pellizcar levemente en los hombros;
si reacciona, seguir la conducta anterior; en
caso de muerte, llamar a los servicios de
emergencias cuanto antes.
Una manera rápida de valorar la conciencia es
determinar si responde o no
Alerta. Está despierto, habla.
Verbal. Responde al llamado, cuando
alzamos la voz y lo llamamos ¡¿Cómo esta?!
Dolor. Responde al dolor, le pellizcamos y
reacciona con gestos o gruñidos.
Inconsciente. No responde.
2. Valoración neurológica mediante la escala
de Glasgow : evaluación de la respuesta
motora
Tiene los ojos abiertos.
a) Nunca. 1
b) Solo al estímulo doloroso. 2
c) Con estímulo verbal. 3
d) De manera espontánea. 4
Respuesta verbal.
a) Sin respuesta. 1
b) No comprensible. 2
c) Incoherencia. 3
d) Habla desorientado. 4
e) Habla orientado. 5
Respuesta motora.
a) Sin respuesta. 1
b) Extensión ante el estímulo. 2
c) Flexión anormal. 3
d) Retira ante estímulos dolorosos. 4
e) Localiza el estímulo doloroso. 5
f) Obedece las órdenes. 6
Valoración de la escala
15 puntos............paciente en estado
normal.
15-14 puntos.........traumatismo
generalizado.
13-9 puntos..........politraumatismo.
inferior a 9 puntos.....traumatismo cráneo-
encefálico grave.
3. Valoración de la respiración.
Nos acercaremos a la boca de la víctima con
la mejilla e intentaremos sentir el aliento a la
vez que dirigimos la mirada al tórax (si
respira se moverá). Es importante destacar
que en caso de que exista respiración, hará
falta explorar el pulso ya que puede o no
tenerlo.
Ver: Miramos el tórax, se eleva o no, si se
eleva y baja respira.
Escuchar: Con el oído escuchamos el sonido
de la respiración.
Sentir: Con los dedos índice y medio
sentimos el pulso carotídeo (a un lado de la
tráquea) de la víctima.
Activar el sistema médico de emergencias o
urgencias.
3. Solicitar ayuda a personal de la emergencia.
4. Valoración del pulso.
Existen múltiples lugares donde buscarlo, se
divide en dos grupos:
Pulso central: Las arterias carótidas, situadas
a ambos lados de la nuez de Adan en una
pequeña depresión, en la garganta; para
sentirlo presionar levemente con los dedos
índice y mayor, nunca con el pulgar
(sentiríamos nuestro propio pulso). Las
arterias femorales, situadas en la región
inguinal, en la raíz del muslo. Sentiremos el
pulso en nuestros dedos.
Pulso periférico: Otros lugares para identificar
el pulso pueden ser las arterias radiales, en la
cara externa de la muñeca. Menos
recomendables ya que en caso de accidente y
pérdida del conocimiento, la sangre se
redistribuye hacia los órganos vitales, y no a
las extremidades por lo que a veces este
método puede resultar engañoso.
En caso de no encontrar pulso, iniciar el
masaje cardiaco, es decir la reanimación
cardiopulmonar RCP.
Según las nuevas pautas de ERC ( European
Resuscitation Council) que se publicaron en
2010 el pulso no es un criterio para decidir
sobre empezar la reanimación
cardiopulmonar.En lugar de eso, la respiración
es más importante porque es más fácil
verificar si una persona respira. [1] . Ademáa
dicen estas Guías que los reanimadores
entrenados deberían también proporcionar
ventilaciones con una relación compresiones-
ventilaciones (CV) de 30:2. Para los
reanimadores no entrenados, se fomenta la
RCP con sólo compresiones torácicas guiada
por teléfono.
Balanza electrónica
Las balanzas electrónicas son balanzas
caracterizadas porque realizan el pesaje
mediante procedimientos que implican sensores .
Las mismas se establecen como una alternativa a
las balanzas de índole mecánica, que tiene el
mismo cometido pero se fundamentan en un
juego de contrapesos. Las balanzas electrónicas
pueden llegar a tener una exactitud notable y un
precio razonable, hecho que las posiciona muy
bien en el mercado. Como contrapartida, pueden
sufrir una mala calibración momentánea,
circunstancia que haría necesario un trabajo de
mantenimiento. Las balanzas electrónicas suelen
ser muy prácticas para la medición de pequeños
pesos, como aquellos que responden a
necesidades de comercialización de productos
para alimentación.
Las balanzas son un elemento que puede
encontrarse ya en épocas remotas. En este caso,
armaban un sistema de contrapesos para conocer
cuánto pesaba un objeto determinado. Así, tenían
dos platillos, uno en donde se ponía un peso
conocido y otra en donde se ponía un peso
desconocido; cuando se equilibrasen los platillos,
se conocería el peso del producto que se buscaba
evaluar. Con pequeñas diferencias, el mismo
principio se usó una y otra vez en las balanzas
mecánicas, cada vez con un mayor grado de
precisión. No obstante, con los adelantos
técnicos, la balanza electrónica vino a ofrecer
una alternativa a este viejo sistema.
La balanza electrónica, a diferencia de su
antecesora, utiliza un sensor para conocer el valor
del peso que se deposita. El mismo envía
distintas señales eléctricas en función del peso,
señales que serán digitalizadas y decodificadas
por un pequeño procesador. El valor resultante
será mostrado en una pequeña pantalla LCD. Es
por ello que este tipo de elementos necesitan
electricidad para su funcionamiento. Si la balanza
está calibrada, la exactitud puede ser muy aguda,
hecho que hace de este tipo de elementos muy
valiosos para distintos ámbitos posibles de
trabajo.
El surgimiento de un artefacto como la balanza
dista de ser accidental. En efecto, ya desde
tiempos remotos existía una necesidad concreta
que satisfacer, la de tener una referencia exacta
de los distintos pesos para poder comerciar
distintos productos. Este hecho hizo que la
medición sea cada vez más precisa. Hoy en día,
con las modernas balanzas digitales, esa
intención primigenia se ve satisfecha en buena
medida y con posibilidades futuras de mejora.
Quizá el único problema de las mismas es la
descalibración que pueden sufrir en determinadas
circunstancias; no obstante, siempre existirán
variantes mejor diseñadas como para hacer más
improbable este tipo de inconveniente.
Cristalización
En los resultados se observa como la pastilla al
ser calentada llega a su punto de ebullición y se
evapora directamente delestado sólido al estado
gaseoso sin pasar por el estado líquido a este
proceso se le llama sublimación. El gas emitido
por el cambio de estado se condensa en una
zona más fría,en este caso la capsula de
porcelana, formando cristales , este proceso se
conoce como cristalización , la cristalización es
”un proceso por el cual a partir de un gas,
unlíquido o una disolución los iones , átomos o
moléculas establecen enlaces hasta formar una
red cristalina”.
Conclusión:
El objetivo de esta práctica fue identificar
lasublimación y deposición como un cambio de
estado , los objetivos de esta práctica fueron
completados con éxito ya que apreciamos la
sublimación con la pastilla de baño , nos queda
claroque la sublimación es el proceso que
consiste en el cambio de estado del estado sólido
al estado gaseoso sin pasar por el estado líquido,
y que la disposición es pasar del estadogaseoso
al estado solido , en esta practica lo vimos con la
cristalización.
Balanza analítica
Una balanza analítica es una clase de balanza
de laboratorio diseñada para medir pequeñas
masas, en un principio de un rango menor del
miligramo (y que hoy día, las digitales, llegan
hasta la diezmilésima de gramo: 0,00001 g o
0,01 mg). Los platillos de medición de una
balanza analítica están dentro de una caja
transparente provista de puertas para que no
se acumule el polvo y para evitar que cualquier
corriente de aire en la habitación afecte al
funcionamiento de la balanza. (A este recinto
a veces se le llama protector de corriente,
draft shield ). El uso de un cierre de seguridad
con ventilación equilibrada, con perfiles
aerodinámicos acrílicos diseñados
exclusivamente a tal fin, permite en el interior
un flujo de aire continuo sin turbulencias que
evita las fluctuaciones de la balanza y que se
puedan medida de masas por debajo de 1 μg
sin fluctuaciones ni pérdidas de producto. Además, la muestra debe estar
a temperatura ambiente para evitar que la
convección natural forme corrientes de aire
dentro de la caja que puedan causar un error
en la lectura.
La balanza analítica electrónica mide la fuerza
necesaria para contrarrestar la masa que está
siendo medida en lugar de utilizar masas
reales. Por ello deben tener los ajustes de
calibración necesarios realizados para
compensar las diferencias gravitacionales.
Utilizan un electroimán para generar la fuerza
que contrarreste la muestra a medir y da el
resultado midiendo la fuerza necesaria para
equilibrar la balanza. Tal dispositivo de
medición se denomina sensor de restauración
de fuerza electromagnética.
Fue desarrollada alrededor de 1750 por el
químico escocés Joseph Black y al ser mucho
más precisa que cualquier otra balanza de la
época, se convirtió en un importante
instrumento científico en la mayoría de los
laboratorios de química.
domingo, 14 de septiembre de 2014
Principios básicos para la prevención y extinción de incendios
¿Que es el fuego?
Se llama fuego a la reacción química de
oxidación violenta de una materia combustible,
con desprendimiento de llamas, calor y gases.
Es un proceso exotérmico. Las llamas son las
partes del fuego que emiten luz visible
Tipos de fuego
En nuestro país, la Norma del Instituto Nacional
de Normalización, clasifica los fuegos en cuatro
clases, y le asigna a cada clase un símbolo
especial. Estos símbolos aparecen en los
extintores, y permiten determinar si el extintor es
apropiado para el tipo de fuego al que se desea
aplicarlo. Estas clases son:
Fuego clase "A"
Los fuegos clase A son aquellos que se producen
en materias combustibles comunes sólidas, como
madera, papeles, cartones, textiles, plásticos, etc.
Cuando estos materiales se queman, dejan
residuos en forma de brasas o cenizas.
El símbolo que se usa es la letra A, en color
blanco, sobre un triángulo con fondo verde
Fuego clase "B"
Los fuegos clase B son los que se producen en
líquidos combustibles inflamables, como petróleo,
gasolina, pinturas, etc. También se incluyen en
este grupo el gas licuado de petróleo y algunas
grasas utilizadas en la lubricación de máquinas.
Estos fuegos, a diferencia de los anteriores, no
dejan residuos al quemarse.
Su símbolo es una letra B, en color blanco, sobre
un cuadrado con fondo rojo.
Fuego clase "C"
Los fuegos clase C son los que comúnmente
identificamos como "fuegos eléctricos". En forma
más precisa, son aquellos que se producen en
"equipos o instalaciones bajo carga eléctrica", es
decir, que se encuentran energizados.
Su símbolo es la letra C, en color blanco, sobre
un círculo con fondo azul.
Cuando en un fuego de clase C se desconecta la
energía eléctrica, éste pasará a ser A, B ó D,
según los materiales involucrados. Sin embargo,
con frecuencia es muy difícil tener la absoluta
certeza de que realmente se ha "cortado la
corriente". En efecto, aunque se haya desactivado
un tablero general, es posible que la instalación
que arde esté siendo alimentada por otro circuito.
Por lo tanto, deberá actuarse como si fuera fuego
C mientras no se logre total garantía de que ya
no hay electricidad.
Fuego clase "D"
Los fuegos clase D son los que se producen en
polvos o virutas de aleaciones de metales livianos
como aluminio, magnesio, etc.
Su símbolo es la letra D, de color blanco, en una
estrella con fondo amarillo.
TIPOS DE EXTINTORES
jueves, 11 de septiembre de 2014
Frases R y S
Que son las frases R y s?
Las Frases de riesgo y de seguridad, también
conocidas como frases R/S , son un sistema de
códigos de riesgo y frases para describir los
riesgos de los compuestos químicos
peligrosos. Las frases R/S consisten de frases
indicadoras de riesgos específicos ( R ) y
consejos de seguridad ( S ). Estas letras son
seguidas de un número, cuya combinación
tiene el mismo significado en diferentes
idiomas .
HUERTAS HDP
Ejemplo
Las frases R/S para ácido clorhídrico en forma
gaseosa (37%) es:
R: 34-37 S: 26-36-45.
Las frases correspondientes idioma español
son:
Riesgos
R34 Provoca quemaduras
R37 Irrita las vías respiratorias
Seguridad
S26 En caso de contacto con los ojos,
lávense inmediata y abundantemente
con agua y acúdase a un médico
S36 Úsese indumentaria protectora
adecuada
S45 En caso de accidente o malestar,
acúdase inmediatamente al médico (si
es posible, muéstresele la etiqueta)
Los guiones separan los números de las frases
distintas.
Ejemplo: R34-37 Provoca quemaduras,
irrita las vías respiratorias
Las barras indican combinaciones de frases
únicas.
Ejemplo: R36/37/38 Irrita los ojos, la piel y
las vías respiratorias
FRASES R
R1- Explosivo en estado seco.
R2- Riesgo de explosión por choque,
fricción, fuego u otras fuentes de ignición.
R3- Alto riesgo de explosión por choque,
fricción, fuego u otras fuentes de ignición.
R4- Forma compuestos metálicos
explosivos muy sensibles.
R5- Peligro de explosión en caso de
calentamiento.
R6- Peligro de explosión, en contacto o sin
contacto con el aire.
R7- Puede provocar incendios.
R8- Peligro de fuego en contacto con
materias combustibles.
R9- Peligro de explosión al mezclar con
materias combustibles.
R10- Inflamable.
R11- Fácilmente inflamable.
R12- Extremadamente inflamable.
R14- Reacciona violentamente con el agua.
R15- Reacciona con el agua liberando gases
extremadamente inflamables.
R16- Puede explosionar en mezcla con
sustancias comburentes.
R17- Se inflama espontáneamente en
contacto con el aire.
R18- Al usarlo pueden formarse mezclas
aire-vapor explosivas/inflamables.
R19- Puede formar peróxidos explosivos.
R20- Nocivo por inhalación.
R21- Nocivo en contacto con la piel.
R22- Nocivo por ingestión.
R23- Tóxico por inhalación.
R24- Tóxico en contacto con la piel.
R25- Tóxico por ingestión.
R26- Muy tóxico por inhalación.
R27- Muy tóxico en contacto con la piel.
R28- Muy tóxico por ingestión.
R29- En contacto con agua libera gases
tóxicos.
R30- Puede inflamarse fácilmente al usarlo.
R31- En contacto con ácidos libera gases
tóxicos.
R32- En contacto con ácidos libera gases
muy tóxicos.
R33- Peligro de efectos acumulativos.
R34- Provoca quemaduras.
R35- Provoca quemaduras graves.
R36- Irrita los ojos.
R37- Irrita las vías respiratorias.
R38- Irrita la piel.
R39- Peligro de efectos irreversibles muy
graves.
R40- Posibles efectos cancerígenos.
R41- Riesgo de lesiones oculares graves.
R42- Posibilidad de sensibilización por
inhalación.
R43- Posibilidad de sensibilización en
contacto con la piel.
R44- Riesgo de explosión al calentarlo en
ambiente confinado.
R45- Puede causar cáncer.
R46- Puede causar alteraciones genéticas
hereditarias.
R48- Riesgo de efectos graves para la salud
en caso de exposición prolongada.
R49- Puede causar cáncer por inhalación.
R50- Muy tóxico para los organismos
acuáticos.
R51- Tóxico para los organismos acuáticos.
R52- Nocivo para los organismos acuáticos.
R53- Puede provocar a largo plazo efectos
negativos en el medio ambiente acuático.
R54- Tóxico para la flora.
R55- Tóxico para la fauna.
R56- Tóxico para los organismos del suelo.
R57- Tóxico para las abejas.
R58- Puede provocar a largo plazo efectos
negativos en el medio ambiente.
R59- Peligroso para la capa de ozono.
R60- Puede perjudicar la fertilidad.
R61- Riesgo durante el embarazo de efectos
adversos para el feto.
R62- Posible riesgo de perjudicar la
fertilidad.
R63- Posible riesgo durante el embarazo de
efectos adversos para el feto.
R64- Puede perjudicar a los niños
alimentados con leche materna.
R65- Nocivo: si se ingiere puede causar
daño pulmonar.
R66- La exposición repetida puede provocar
sequedad o formación de grietas en la piel.
R67- La inhalación de vapores puede
provocar somnolencia y vértigo.
R68- Posibilidad de efectos irreversibles.
FRASES S
S1- Consérvese bajo llave.
S2- Manténgase fuera del alcance de los
niños.
S3- Consérvese en lugar fresco.
S4- Manténgase lejos de locales
habilitados.
S5- Consérvese en ... (líquido apropiado a
especificar por el fabricante)
S6- Consérvese en ... (gas inerte a
especificar por el fabricante) .
S7- Manténgase el recipiente bien cerrado.
S8- Manténgase el recipiente en lugar seco.
S9- Consérvese el recipiente en lugar bien
ventilado.
S12- No cerrar el recipiente
herméticamente.
S13- Manténgase lejos de alimentos,
bebidas y piensos.
S14- Consérvese lejos de ... (materiales
incompatibles a especificar por el fabricante) .
S15- Conservar alejado del calor.
S16- Conservar alejado de toda llama o
fuente de chispas-No fumar.
S17- Manténgase lejos de materiales
combustibles.
S18- Manipúlese y ábrase el recipiente con
prudencia.
S20- No comer ni beber durante su
utilización.
S21- No fumar durante su utilización.
S22- No respirar el polvo.
S23- No respirar los gases/humos/vapores/
aerosoles [denominación(es) adecuada(s) a
especificar por el fabricante] .
S24- Evítese el contacto con la piel.
S25- Evítese el contacto con los ojos.
S26- En caso de contacto con los ojos,
lávense inmediata y abundantemente con agua
y acúdase a un médico.
S27- Quítese inmediatamente la ropa
manchada o salpicada.
S28- En caso de contacto con la piel, lávese
inmediata y abundantemente con ...
(productos a especificar por el fabricante) .
S29- No tirar los residuos por el desagüe.
S30- No echar jamás agua a este producto.
S33- Evítese la acumulación de cargas
electrostáticas.
S35- Elimínense los residuos del producto y
sus recipientes con todas las precauciones
posibles.
S36- Úsese indumentaria protectora
adecuada.
S37- Úsense guantes adecuados.
S38- En caso de ventilación insuficiente,
úsese equipo respiratorio adecuado.
S39- Úsese protección para los ojos/la
cara.
S40- Para limpiar el suelo y los objetos
contaminados por este producto, úsese ... (a
especificar por el fabricante) .
S41- En caso de incendio o de explosión no
respire los humos.
S42- Durante las fumigaciones/
pulverizaciones, úsese equipo respiratorio
adecuado. [Denominación(es) adecuada(s) a
especificar por el fabricante] .
S43- En caso de incendio, utilizar ... (los
medios de extinción los debe especificar el
fabricante) . (Si el agua aumenta el riesgo, se
deberá añadir: «No usar nunca agua») .
S45- En caso de accidente o malestar,
acúdase inmediatamente al médico (si es
posible, muéstrele la etiqueta).
S46- En caso de ingestión, acúdase
inmediatamente al médico y muéstrele la
etiqueta o el envase.
S47- Consérvese a una temperatura no
superior a ... °C (a especificar por el
fabricante).
S48- Consérvese húmedo con ... (medio
apropiado a especificar por el fabricante).
S49- Consérvese únicamente en el
recipiente de origen.
S50- No mezclar con ... (a especificar por el
fabricante) .
S51- Úsese únicamente en lugares bien
ventilados.
S52- No usar sobre grandes superficies en
locales habitados.
S53- Evítese la exposición-recábense
instrucciones especiales antes del uso.
S56- Elimínense esta sustancia y su
recipiente en un punto de recogida pública de
residuos especiales o peligrosos.
S57- Utilícese un envase de seguridad
adecuado para evitar la contaminación del
medio ambiente.
S59- Remitirse al fabricante o proveedor
para obtener información sobre su
recuperación/reciclado.
S60- Elimínense el producto y su recipiente
como residuos peligrosos.
S61- Evítese su liberación al medio
ambiente. Recábense instrucciones específicas
de la ficha de datos de seguridad.
S62- En caso de ingestión no provocar el
vómito: acúdase inmediatamente al médico y
muéstrele la etiqueta o el envase.
S63- En caso de accidente por inhalación,
alejar a la víctima fuera de la zona
contaminada y mantenerla en reposo.
S64- En caso de ingestión, lavar la boca con
agua (solamente si la persona esta
consciente).
Normas de seguridad e higiene en el laboratorio
Normas referentes a la
instalación
1.
Las ventanas y puertas han de abrir
adecuadamente, ya que en caso de humos
excesivos es necesaria la máxima ventilación y
en caso de incendio, la mínima.
2.
Las mesas, sillas taburetes, suelos, etc., y el
mobiliario en general deben estar en buen
estado para evitar accidentes.
3.
Los grifos de agua y los desagües no deben
tener escapes que hagan resbaladizo el suelo y
pudran la madera. Los desagües deben
permitir bien el paso de agua.
4.
Los enchufes o cables eléctricos no deben
estar rotos o pelados; en caso de que sea así
deben sustituirse inmediatamente o
protegerse para que no puedan tocarse. Nunca
deben ir por el suelo de forma que se puedan
pisar.
5.
Los armarios y estanterías deben ofrecer un
almacenamiento para aparatos y productos
químicos y estar siempre en perfecto orden.
Normas personales
1.
Cada grupo se responsabilizará de su zona de
trabajo y de su material.
2.
La utilización de bata es muy conveniente, ya
que evita que posibles proyecciones de
sustancias químicas lleguen a la piel.
3.
Es muy aconsejable, si se tiene el pelo largo,
llevarlo recogido o metido en la ropa, así como
no llevar colgantes.
4.
En el laboratorio no se podrá fumar, ni tomar
bebidas ni comidas.
Normas referentes al orden
1.
Las sustancias tóxicas permanecerán en
armario con llave.
2.
Es imprescindible la limpieza del laboratorio,
de su instrumental y utensilios, así como que
esté ordenado.
3.
En las mesas de laboratorio o en el suelo, no
pueden depositarse prendas de vestir,
apuntes, etc., que pueden entorpecer el
trabajo.
Normas referentes a la
utilización de productos
químicos
1.
Antes de utilizar un determinado compuesto,
asegurarse bien de que es el que se necesita;
para ello leeremos, si es preciso un par de
veces, el rótulo que lleva el frasco.
2.
Como regla general, no coger ningún producto
químico. El profesor los proporcionará.
3.
No devolver nunca a los frascos de origen los
sobrantes de los productos utilizados sin
consultar al profesor.
4.
Es de suma importancia que cuando los
productos químicos de desecho se viertan en
las pilas de desagüe, aunque estén
debidamente neutralizados, enseguida circule
por el mismo abundante agua.
5.
No tocar con las manos, y menos con la boca,
los productos químicos.
6.
No pipetear con la boca los productos
abrasivos. Utilizar la bomba manual o una
jeringuilla.
7.
Los ácidos requieren un cuidado especial.
Cuando queramos diluirlos, nunca echaremos
agua sobre ellos; siempre al contrario, es
decir, ácido sobre el agua.
8.
Los productos inflamables no deben estar
cerca de fuentes de calor, como estufas,
hornillos, radiadores, etc.
9.
Cuando se vierta cualquier producto químico
debe actuarse con rapidez, pero sin
precipitación.
10.
Si se vierte sobre tí cualquier ácido o producto
corrosivo, lávate inmediatamente con mucha
agua y avisa al profesor.
11.
Al preparar cualquier disolución, se colocará
en un frasco limpio y rotulado
convenientemente.
Normas referentes a la
utilización del material de
vidrio
1.
Cuidado con los bordes y puntas cortantes de
tubos u objetos de vidrio. Alisarlos al fuego.
Mantenerlos siempre lejos de los ojos y de la
boca.
2.
El vidrio caliente no se diferencia a simple
vista del vidrio frío. Para evitar quemaduras,
dejarlo enfriar antes de tocarlo (sobre ladrillo,
arena, planchas de material aislante,...).
3.
Las manos se protegerán con guantes o trapos
cuando se introduzca un tapón en un tubo de
vidrio.
Normas referentes a la
utilización de balanzas
1.
Cuando se determinen masas de productos
químicos con balanzas, se colocará papel de
filtro sobre los platos de la misma y, en
ocasiones, será necesario el uso de un "vidrio
de reloj" para evitar el ataque de los platos por
parte de sustancias corrosivas.
2.
Se debe evitar cualquier perturbación que
conduzca a un error, como vibraciones
debidas a golpes, aparatos en funcionamiento,
soplar sobre los platos de la balanza, etc.
Normas referentes a la
utilización de gas
1.
El uso del gas butano requiere un cuidado
especial: si se advierte su olor, cerrar la llave
y avisar al profesor.
2.
Si se vierte un producto inflamable, córtese
inmediatamente la llave general de gas y
ventilar muy bien el local.
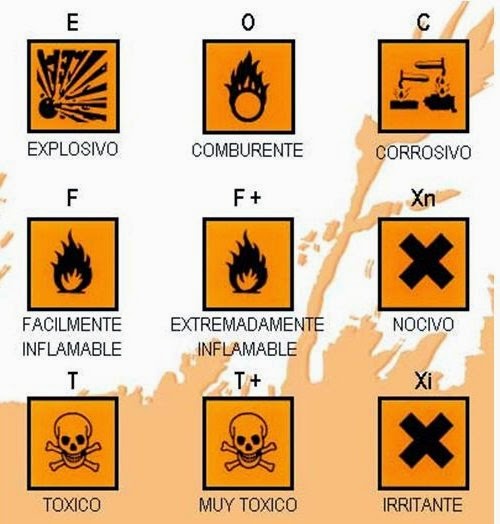
Sustancias químicas peligrosas
Las sustancias químicas se clasifican, en
función de su peligrosidad, en:
Explosivos.
Sustancias y preparados que pueden
explosionar bajo el efecto de una llama.
Comburentes.
Sustancias y preparados que, en contacto con
otros, particularmente con los inflamables,
originan una reacción fuertemente
exotérmica.
Extremadamente inflamables.
Sustancias y productos químicos cuyo punto
de ignición sea inferior a 0°C, y su punto de
ebullición inferior o igual a 35°C.
Fácilmente inflamables.
Se definen como tales:
Sustancias y preparados que, a la temperatura
ambiente, en el aire y sin aporte de energía,
puedan calentarse e incluso inflamarse.
Sustancias y preparados en estado líquido con
un punto de ignición igual o superior a 0°C e
inferior a 21°C.
Sustancias y preparados sólidos que puedan
inflamarse fácilmente por la acción breve de
una fuente de ignición y que continúen
quemándose o consumiéndose después del
alejamiento de la misma.
Sustancias y preparados gaseosos que sean
inflamables en el aire a presión normal.
Sustancias y preparados que, en contacto con
el agua y el aire húmedo, desprendan gases
inflamables en cantidades peligrosas.
Inflamables.
Sustancias y preparados cuyo punto de
ignición sea igual o superior a 21°C e inferior
a 55°C.
Muy tóxicos.
Sustancias y preparados que por inhalación,
ingestión o penetración cutánea puedan
entrañar riesgos graves, agudos o crónicos, e
incluso la muerte.
Nocivos.
Sustancias y preparados que por inhalación,
ingestión o penetración cutánea puedan
entrañar riesgos de gravedad limitada.
Corrosivos.
Sustancias y preparados que en contacto con
los tejidos vivos puedan ejercer sobre ellos
una acción destructiva.
Irritantes.
Sustancias y preparados no corrosivos que por
contacto inmediato, prolongado o repetido con
la piel o mucosas pueden provocar una
reacción inflamatoria.
Peligrosos para el medio ambiente.
Sustancias y preparados cuya utilización
presente o pueda presentar riesgos inmediatos
o diferidos para el medio ambiente.
Carcinógenos.
Sustancias y preparados que por inhalación,
ingestión o penetración cutánea puedan
producir cáncer o aumento de su frecuencia.
Teratogénicos.
Sustancias y preparados que por inhalación,
ingestión o penetración cutánea puedan
inducir lesiones en el feto durante su
desarrollo intrauterino.
Mutagenicos .
Sustancias y preparados que por inhalación,
ingestión o penetración cutánea puedan
producir alteraciones en el material genético
de las células.
Algunas de estas sustancias se reflejan en el
etiquetado de los productos químicos
mediante un símbolo o pictograma, de manera
que se capte la atención de la persona que va
a utilizar la sustancia.
Algunos instrumentos de laboratorio
¿Que son los materiales de laboratorio?
Son Aparatos destinados a la
cualificacion y/o cuantificacion de
sustancias quimicas, utilizando diversos
metodos.
Ejemplos: Potenciometro, Espectrofotometro
ultravioleta, visible, Infrarrojo,
Cromatografia de gases, Cromatografia Gas-
liquido, Liquido-Liquido, Resonancia
magnetica Nuclear, absorcion atomica. Pero
estos no se podrian utilizar sin los
materiales de laboratorio. Balanza analitica.
En un laboratorio de química se utilizan
diversos materiales de laboratorio. A
aquellos que se utilizan para medir
volúmenes se los clasifica como Material
volumétrico.
La mayoría están constituidos por vidrio
para permitir la visualización del líquido
que se desea medir. Aunque en algunos
casos se utilizan de plástico transparente, ya
sea por su bajo precio, o para evitar una
reacción entre el líquido y el vidrio (por
ejemplo cuando se mide ácido fluorhídrico).
Pero debe tenerse en cuenta que, en
general, tienen una precisión menor.
Subclasificación:A fin de medir el volumen
poseen unas marcas grabadas. Se puede
subclasificar el material según el formato de
estas marcas.
Material volumétrico graduado
En este caso el elemento posee una
graduación, una serie de líneas que indican
diferentes volúmenes.
Material volumétrico aforado
Posee uno o más aforos.
Hay otra subclasificación que pueden recibir
algunos de estos materiales, por ejemplo las
pipetas y buretas (tanto las graduadas como
las aforadas), pero no las probetas.
de simple enrase/aforo
En este caso, los 0 ml corresponden al
elemento vacío (en realidad, se tiene en
cuenta que siempre quedan unas gotas). En
este caso deberá enrasarse una sola vez.
de doble enrase/doble aforo
En este caso, existe una marca para el los 0
ml. Tiene como desventajas que es necesario
enrasar dos veces (una al principio, y otra al
final de la medición); y que si por error
seguimos vertiendo el líquido más allá de la
marca podemos arruinar el trabajo hecho. Y
tiene la ventaja de poder utilizarse si se
rompe la punta, mientras que no llegue a la
marca de 0 ml.
Metodología de uso:Si quieres saber cómo
se miden los volúmenes de la mayoría de los
materiales, puedes consultar cómo enrasar.
Al margen de esto, el material volumétrico
debe usarse con cuidado:
No se lo debe exponer a variaciones bruscas
o amplias de temperatura. Generalmente
indican el rango de temperatura en el que
puede operarse.
Tener un manejo cuidadoso, ya que son muy
frágiles. Esto incluye también no apoyarla
horizontalmente sobre superficies que
pueden estar inclinadas, ni muy cerca de
elementos de metal que puedan romperlo.
Materiales comprendidos:]Bureta
Matraz
Erlenmeyer
Matraz aforado
Pipeta
Probeta
Como usar el mechero bunsen
Paso 1
Conecta el mechero Bunsen a una fuente o llave
de gas usando tubería de caucho. Examina de
antemano la tubería para asegurarte de que no
tenga agujeros.
Paso 2
Gira el collar en la posición inferior del mechero
Bunsen de forma que los agujeros de éste
queden ligeramente abiertos.
Paso 3
Con cuidado, enciende un fósforo. Asegúrate de
tomarlo con firmeza y mantén tus dedos lejos de
la llama para evitar quemaduras.
Paso 4
Abre la llave del gas. Para hacer ésto, oprime y
gira la boquilla de forma que quede paralela con
la llave o tubería del gas, lo cual permitirá que el
gas fluya al mechero Bunsen.
Paso 5
Mueve el fósforo encendido sobre la parte
superior del mechero para encenderlo. Haz ésto
con mucho cuidado, asegurándote de que el
cerillo no se apague antes de que el mechero
Bunsen se encienda.
Paso 6
Ajusta los agujeros del mechero usando el collar
hasta que obtengas la llama apropiada. Por lo
regular, querrás que la llama sea azul, lo cual
puedes conseguir abriendo por completo o casi
por completo los agujeros del mechero Bunsen.